Emular en el laboratorio el comportamiento de un tumor alojado en un chip impreso en 3D, con un tamaño menor a una moneda de un cuarto de dólar, al cultivar sus células a microescala y evaluar el efecto de diferentes fármacos, podría ser el camino hacia una medicina personalizada para quienes padecen cáncer.
En pacientes diagnosticados con esta enfermedad, la tecnología de tumor en un chip (ToC) podría significar no solo una reducción de costos en la búsqueda de una cura, sino la posibilidad de recibir un tratamiento que se ajuste a sus necesidades, con fármacos que ataquen con mayor precisión el tejido canceroso y con una menor cantidad de efectos adversos, dice Salvador Gallegos, quien durante sus estudios de doctorado en Biotecnología en el Tec y ahora como investigador en Harvard ha trabajado con estos dispositivos.
Los tumores en chips son plataformas útiles para estudiar la fisiología de los tejidos cancerosos y evaluar la eficacia y toxicidad de los fármacos contra la enfermedad, explica. “En la literatura a esta tecnología también se le conoce como sistemas microfisiológicos y son plataformas de cultivo celular en escala micro −y a veces nano− que utilizan la microfluídica para hacer crecer tejidos y exponerlos a fármacos”, explica el investigador.
El tipo y diseño del órgano o cáncer en chip dependerá de su uso, ya sea para evaluación de fármacos o para modelar diferentes tipos de enfermedades como cáncer de pulmón, mama o colorrectal, entre otras.

Tumor en un chip: un paso hacia la medicina personalizada
A finales de 2020, el gobierno de Estados Unidos aprobó la Ley de Modernización 2.0 de la Administración de Alimentos y Medicamentos (FDA), que contempla el uso de órganos en chip como alternativa a los ensayos con animales en las pruebas para evaluar fármacos.
Gallegos señala que, además de ensayos con ratones, conejos y otros animales, están las pruebas de cultivo 2D, donde las células se desarrollan en placas de plástico monocapa, sin embargo, en ambos casos, ninguna de las plataformas se asemeja al comportamiento que ocurre en el cuerpo humano.
“Al momento de querer extrapolar esos resultados, se ve que son discrepantes, no hay concordancia; ahí surge la inspiración de un cáncer en un chip, hacer en el laboratorio un modelo más robusto, predecible al momento de probar fármacos y que cuando los vayas a exponer a un paciente tengas la certeza de que sean más eficaces, eso es medicina personalizada”, señala Gallegos.
Para el desarrollo de tratamientos personalizados es necesario obtener células de los pacientes a través de una biopsia, luego son cultivadas en un sistema microfluídico, suspendidas en un hidrogel −un polímero con elasticidad y porosidad similar a los tejidos naturales para la oxigenación y entrada de nutrientes− y se les hace crecer para probar los fármacos.
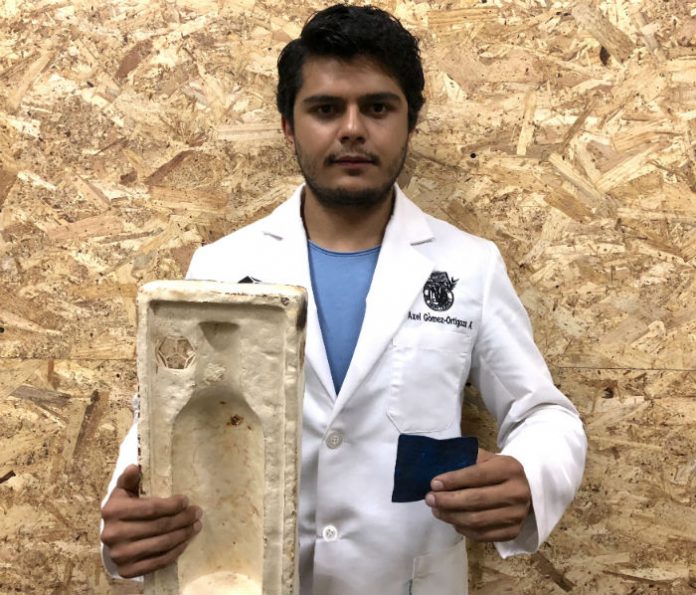
Los órganos o tumores en chip tienen un tamaño menor a los 30 milímetros y las barreras que conforman su estructura comúnmente pueden ser de dos materiales: resinas poliméricas que se crean con impresoras 3D y un polímero llamado PDMS (polidimetilsiloxano), los cuales son transparentes para que los investigadores puedan ver lo que pasa con las células y son permeables a gases como oxígeno, CO2 y otros necesarios para el crecimiento de estas.
“En el Tec trabajé con cáncer de mama, dirigí esos flujos en un sistema que es un reactor microscópico donde hay una cavidad, como una alberca, donde están las células y a los lados dos canales: uno para alimentar, por el que pasan nutrientes, oxígeno, azúcares y factores de crecimiento, y otro para purgar los desechos, se trata de emular los flujos por los que va la sangre y cómo un tejido o tumor crece fuera del cuerpo”, señala.
Como parte del Alvarez-Trujillo Lab, el investigador hizo pruebas con fármacos como la doxorubicina y el docetaxel, donde evaluó el transporte del medicamento, su viabilidad y toxicidad, así como el consumo de glucosa y la muerte celular.
Actualmente, el grupo de investigadores se apoya en los tumores en chip para estudiar otros tipos de cáncer, como el colorrectal, de pulmón y de próstata.
Probar fármacos en un órgano en chip no tiene implicaciones éticas, señala Gallegos, pues las evaluaciones se realizan en las células independientes que se hacen en el laboratorio y no en un cuerpo humano, únicamente sería necesario contar con el consentimiento informado del paciente.
Beneficios para pacientes y empresas farmacéuticas
El desarrollo de la tecnología de tumores en chip puede significar para los pacientes la posibilidad de reducir costos en tratamiento, dice Gallegos, pues “la inversión principal sería al principio, para el diseño del análisis y la validación, ya teniendo eso lo demás es muy accesible económicamente, porque con la plataforma lista solo hay que cultivar las células y correr varias pruebas, simultáneamente, como se hacía con la detección de COVID”.
Al contar con células del paciente y dependiendo de sus características fisiológicas, químicas y genéticas, será posible personalizar tratamientos con fármacos que ataquen de manera más óptima un determinado tipo de cáncer.
A su vez, se podrían reducir los efectos secundarios y el tiempo necesario para probar uno o varios fármacos de los tratamientos que hoy se acostumbran para tratar la enfermedad.
“Recientemente leí un artículo sobre una prueba piloto donde pacientes con cáncer donaron sus biopsias y con sus células se hicieron tumores con chip para que fueran expuestos a fármacos y que se evaluaran, eran pacientes fases avanzadas de cáncer y vieron que cerca del 47% incrementaron entre cinco y 10 años su esperanza de vida”.
El tiempo en el que se realizan las pruebas con fármacos en plataformas de cáncer en chip varía, sin embargo, el promedio para conocer si son tóxicos o no −es decir, que no mata células sanas o promueve el crecimiento del tumor− tarda en promedio dos semanas.
El investigador considera que para las farmacéuticas este tipo de plataformas también representa ahorros millonarios al correr pruebas clínicas e investigación para validar la eficacia de los medicamentos. Incluso, algunas ya comienzan a producir estos dispositivos en serie, pero enfrentan el desafío de la personalización para satisfacer las necesidades particulares de los pacientes.
Actualmente, existen retos para los investigadores que trabajan con órganos o tumores en chip, entre ellos están el ganar la confianza de los médicos para adoptar estos dispositivos al definir tratamientos oncológicos, otro, tiene que ver con lograr una interconexión entre varios de ellos para desarrollar sistemas que puedan replicar el funcionamiento de cuerpo humano.
“Vamos a ver cómo se comportan los órganos en chip al conectarse con otros, ver si se parecen a un sistema vivo, ese es uno de los principales retos, tener una entidad biológica creciendo en el laboratorio para modelar enfermedades y evaluar fármacos”, comenta.
¿Te interesó esta historia? ¿Quieres publicarla? Contacta a nuestra editora de contenidos para conocer más marianaleonm@tec.mx.