Por Sergio Antonio Ayala Mar y José Guillermo González Valdez
Los avances en el campo de los biomateriales están transformando el tratamiento de enfermedades crónicas como la diabetes, además de enfermedades cardiovasculares y el cáncer y con ello cambiando nuestra perspectiva del envejecimiento.
Piensa en un puente que conecta la biología y la ingeniería. Los biomateriales se desarrollan utilizando principios de ingeniería para resolver problemas biológicos. La biología proporciona el contexto y las necesidades específicas del cuerpo humano, mientras que la ingeniería aporta las herramientas y técnicas para crear soluciones innovadoras.
¿Cómo estos materiales y sus diseños cambiarán la forma en la que tratamos las enfermedades?
Avance en biomateriales
Los biomateriales son sustancias utilizadas en medicina para interactuar con el cuerpo humano de manera segura y efectiva. Pueden ser naturales, como el colágeno o la seda, o sintéticos, como ciertos tipos de plásticos o metales. Todos con la posibilidad de utilizarse en implantes, prótesis y dispositivos médicos.
Su principal característica es la biocompatibilidad, es decir, no provocan una reacción adversa significativa. Incluso se investigan aquellos capaces de liberar medicamentos o degradarse después de cumplir su función, mejorando así los tratamientos médicos y la calidad de vida de los pacientes.
La investigación y el desarrollo de biomateriales, diseñados específicamente para interactuar con el cuerpo humano y otros sistemas biológicos, se ha incrementado en las últimas décadas.
Esta tendencia se ha impulsado por avances en nanotecnología, biotecnología e ingeniería de tejidos, convirtiendo a los biomateriales en herramientas fundamentales para la innovación médica.
Hoy en día, las aplicaciones se han expandido considerablemente para incluir dispositivos médicos avanzados, sistemas de liberación de fármacos, prótesis personalizadas y terapias regenerativas.
Según datos recientes del Observatorio Mundial de la Salud de la OMS, la esperanza de vida global ha aumentado a un promedio de 73 años (1). Este aumento en la longevidad está asociado a un incremento en enfermedades crónicas, como las enfermedades cardiovasculares, la diabetes y el cáncer, que afecta la calidad de vida de millones de personas en todo el mundo (2).
El envejecimiento de la población y el consiguiente aumento en enfermedades crónicas son retos importantes que resaltan la necesidad de la innovación médica. El desarrollo de tecnología médica es una oportunidad para abordar estos desafíos, ofreciendo oportunidades de innovación en la prevención, el diagnóstico, y el tratamiento (3,4).
Hidrogeles y exosomas
En este contexto, se llevó a cabo el 12th World Biomaterials Congress (12° Congreso Mundial de Biomateriales), en Daegu, Corea del Sur, evento en el que los biomateriales se presentaron como una solución complementaria para responder a las necesidades médicas actuales y abrir nuevas fronteras en la medicina.
Este evento, que se celebra cada cuatro años, convoca a investigadores e iniciativa privada para presentar y debatir los últimos avances en el campo. En 2024, Corea del Sur —que aspira a convertirse en líder mundial en innovación médica— fue el anfitrión.
En esta edición, investigadores de la Escuela de Ingeniería y Ciencias del Tecnológico de Monterrey, en colaboración con investigadores del Departamento de Ingeniería Biomédica de la Universidad de Illinois en Chicago (UIC), presentamos un trabajo sobre hidrogeles biodegradables para la liberación controlada de exosomas (5).
Los exosomas, pequeñas partículas o vesículas producidas por todas las células del cuerpo, son reconocidos como nanomateriales naturales debido a su tamaño nanométrico y origen celular (6). Estas vesículas tienen la función de transportar moléculas de una célula a otra, lo que los convierte en vehículos ideales para generar nuevas estrategias terapéuticas.
Las terapias basadas en exosomas utilizan estos transportadores para llevar tratamientos directamente a las células enfermas, lo que mejora la eficacia y reduce los efectos secundarios (7).
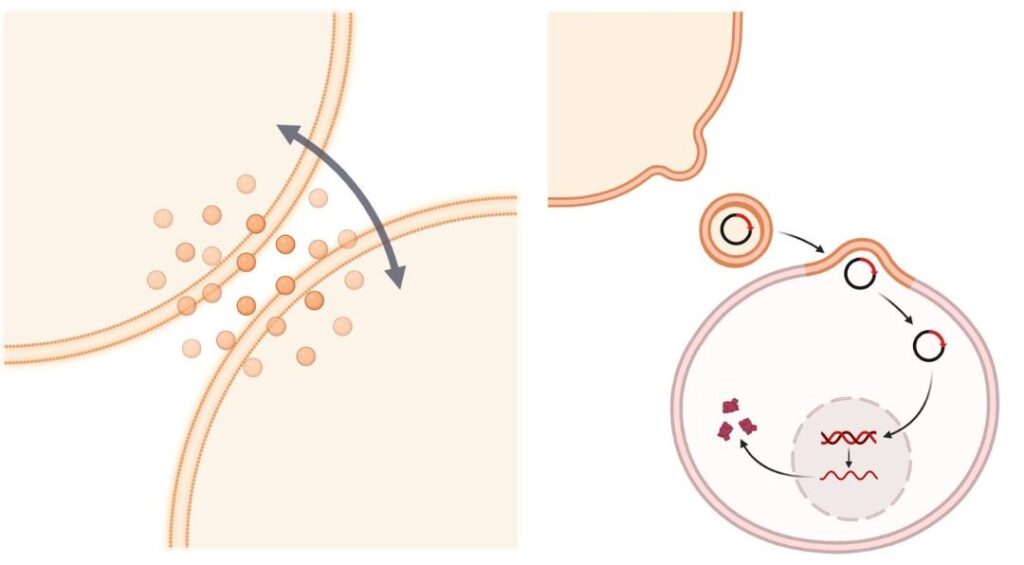
Sin embargo, garantizar que los exosomas lleguen de manera eficiente y específica a los sitios deseados, con el fin de maximizar su efectividad, continúa siendo un desafío significativo (8).
La investigación presentada representa los primeros pasos en el desarrollo de un método que permita que las terapias basadas en exosomas sean entregadas en un sitio específico durante un tiempo determinado.
De esta manera, los hidrogeles emergen como una alternativa atractiva para alcanzar nuestro objetivo. Estos materiales, ya sean naturales o sintéticos, forman una red tridimensional de moléculas que retiene agua sin disolverse completamente, lo que los hace especialmente adecuados para la liberación controlada de tratamientos (9).
Además, los hidrogeles tienen la capacidad de imitar las propiedades del tejido blando humano, actuando como estructuras de soporte para el crecimiento de células en la ingeniería de tejidos, y pueden utilizarse como apósitos o parches para mantener las heridas húmedas y protegidas (10).
Estos materiales poseen la versatilidad de ser inyectados o implantados directamente en el lugar deseado del cuerpo, ya sea en la piel o en internamente. Asimismo, cuando se incorporan moléculas terapéuticas durante su formulación, éstas pueden ser liberadas de manera controlada (10).
El proceso ocurre a medida que el hidrogel absorbe agua y la red tridimensional de moléculas que conforman se degrada, proporcionando una liberación controlada de los agentes terapéuticos en el sitio de administración.
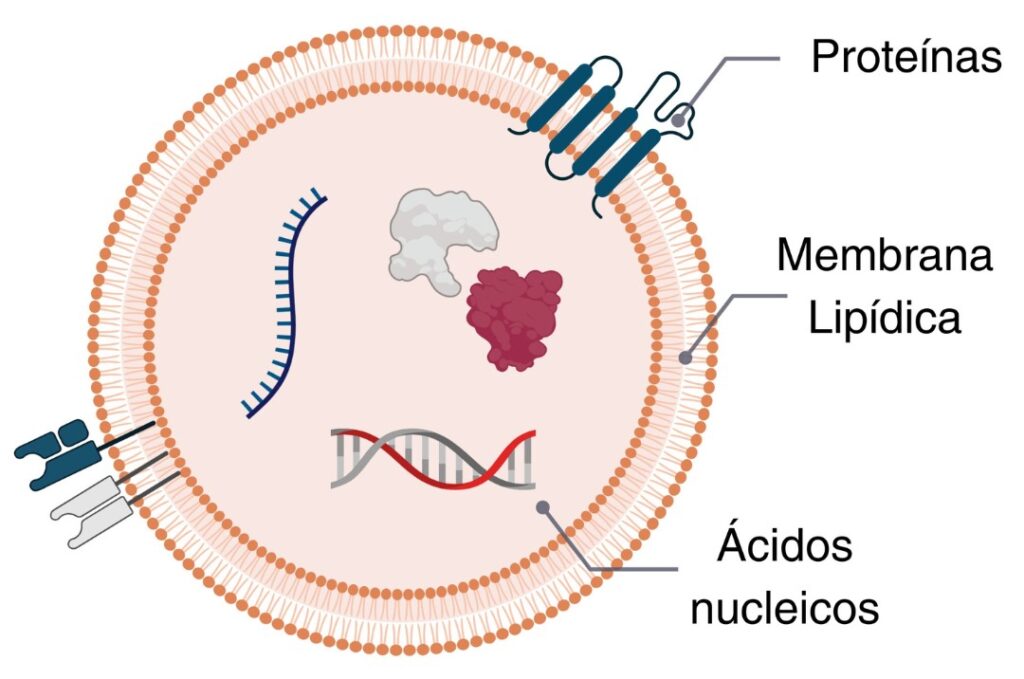
Controlar los exosomas
La investigación se centra en la incorporación de exosomas en hidrogeles compuestos por alginato oxidado y metacrilado (OMA), biomaterial desarrollado por nuestros colaboradores en UIC (11,12).
El alginato, un polímero natural derivado de las algas, es modificado químicamente a través de procesos de oxidación y metacrilación, lo que permite su fotopolimerización con luz ultravioleta (13).
La fotopolimerización ofrece control preciso, rapidez y eficiencia en la producción de hidrogeles. Además, ajustando el grado de oxidación del alginato, podemos manipular la tasa de degradación del hidrogel (14). Esto facilita la liberación de fármacos de manera rápida o sostenida, dependiendo de las necesidades clínicas específicas.
La investigación aprovecha el potencial del alginato oxidado y metacrilado (OMA) para diseñar hidrogeles de forma eficiente y con propiedades personalizables (5,15). Un alto grado de oxidación del alginato provoca una degradación más rápida, facilitando una liberación rápida de exosomas. Por el contrario, un menor grado de oxidación resulta en una degradación más lenta, permitiendo una liberación sostenida de exosomas.
Este enfoque permite una liberación a un ritmo preciso y ofrece la posibilidad de adaptar las formulaciones a las necesidades específicas de cada paciente.
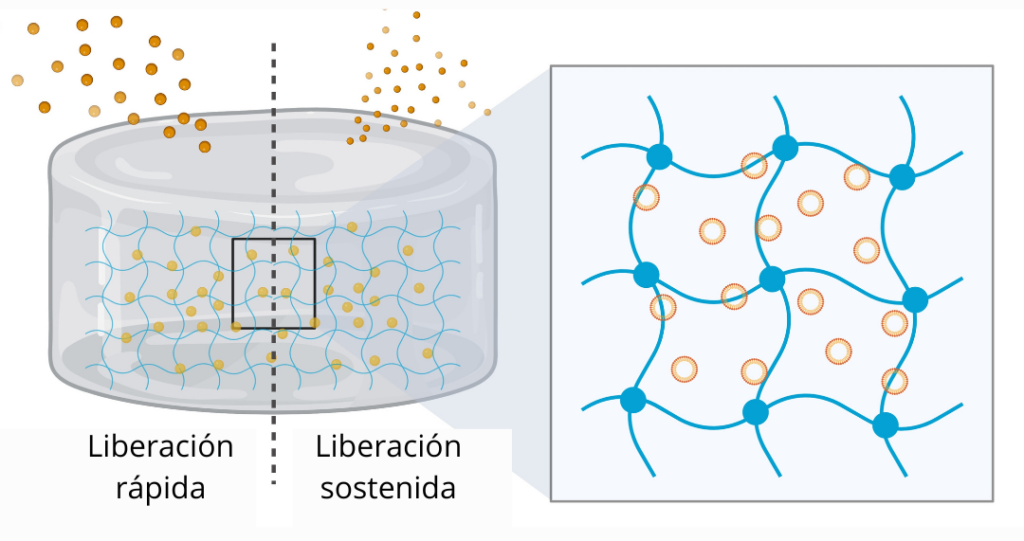
Esta versatilidad es relevante si consideramos que estudios recientes han demostrado que estas técnicas mejoran eficacia en diversos contextos clínicos (16).
En enfermedades cardiovasculares, estos hidrogeles tienen el potencial de reparar tejidos cardíacos dañados después de un infarto, liberando exosomas que estimulan la regeneración celular (17,18).
En el tratamiento de heridas crónicas en pacientes con diabetes, estos hidrogeles actúan como parches que fomentan una recuperación rápida de la piel (19). Además, en el tratamiento del cáncer, pueden implantarse cerca de tumores para liberar exosomas que transporten agentes antitumorales directamente a las células cancerígenas, aumentando la eficacia del tratamiento y reduciendo los efectos secundarios (20).
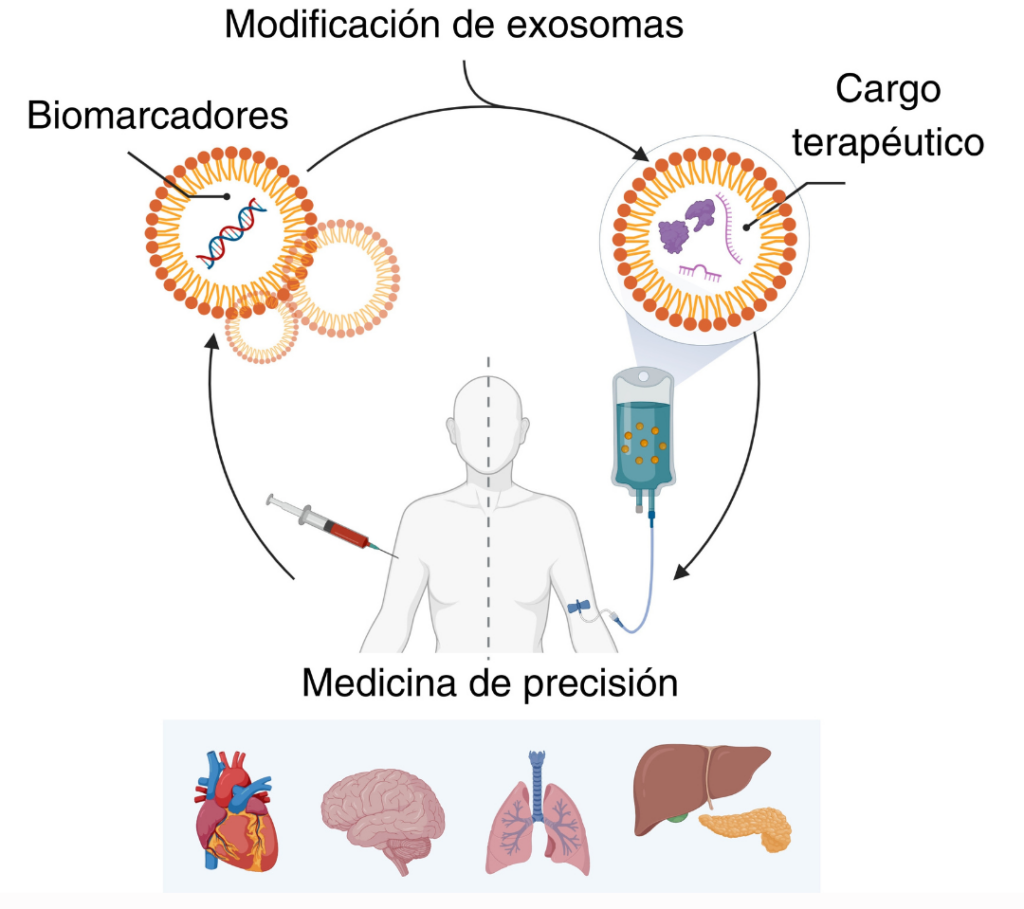
Convergencia en biomateriales
En medicina regenerativa, los biomateriales están diseñados para simular la estructura de soporte de las células en los tejidos. Durante el congreso, se presentaron avances tecnológicos que facilitan la generación de modelos de órganos que son útiles para estudiar cómo se desarrollan las enfermedades y probar nuevos tratamientos (21).
En cardiología, los biomateriales son fundamentales en procedimientos mínimamente invasivos(22). Actualmente, se está trabajando en materiales avanzados para la personalización de implantes cardíacos que se adaptan a las características anatómicas y funcionales de cada paciente (23).
En el sector de la tecnología médica portátil, se destacó el uso de nuevos materiales para desarrollar biosensores (24,25). Estos dispositivos plantean identificar y medir diversas moléculas directamente en el cuerpo humano, permitiendo un seguimiento constante y preciso de parámetros de salud en tiempo real (26,27).
En el campo de la medicina de precisión, se destacaron los nanotransportadores diseñados para la terapia contra el cáncer (28). Estos transportadores están diseñados para reconocer y unirse a células específicas, prometiendo incrementar la eficacia y reducir los efectos secundarios de terapias personalizadas (29). Además, se discutió la adaptación de nanomateriales para la producción de vacunas en regiones con recursos limitados, mejorando el acceso a intervenciones preventivas (30).
El futuro de la medicina está ligado al desarrollo de biomateriales avanzados. La investigación y desarrollo en este campo no solo puede mejorar las terapias actuales, sino que también abre nuevas fronteras para la creación de estrategias que pueden transformar la atención médica.
.
Referencias
- Vardell E. Global Health Observatory Data Repository. Med Ref Serv Q. 2020;39(1):67-74.
- Partridge L, Deelen J, Slagboom PE. Facing up to the global challenges of ageing. Nature. septiembre de 2018;561(7721):45-56.
- De Santis KK, Mergenthal L, Christianson L, Busskamp A, Vonstein C, Zeeb H. Digital Technologies for Health Promotion and Disease Prevention in Older People: Scoping Review. J Med Internet Res. 23 de marzo de 2023;25:e43542.
- Stavropoulos TG, Papastergiou A, Mpaltadoros L, Nikolopoulos S, Kompatsiaris I. IoT Wearable Sensors and Devices in Elderly Care: A Literature Review. Sensors. 16 de mayo de 2020;20(10).
- Ayala Mar SA. Research and development of emerging technologies for exosome-based cancer diagnostics and therapeutics. 2023.
- Kalluri R, LeBleu VS. The biology, function, and biomedical applications of exosomes. Science. febrero de 2020;367(6478):eaau6977-eaau6977.
- Kim HI, Park J, Zhu Y, Wang X, Han Y, Zhang D. Recent advances in extracellular vesicles for therapeutic cargo delivery. Exp Mol Med. 1 de abril de 2024;56(4):836-49.
- Choi H, Choi Y, Yim HY, Mirzaaghasi A, Yoo JK, Choi C. Biodistribution of Exosomes and Engineering Strategies for Targeted Delivery of Therapeutic Exosomes. Tissue Eng Regen Med. agosto de 2021;18(4):499-511.
- Cao H, Duan L, Zhang Y, Cao J, Zhang K. Current hydrogel advances in physicochemical and biological response-driven biomedical application diversity. Signal Transduct Target Ther. 16 de diciembre de 2021;6(1):426.
- Correa S, Grosskopf AK, Lopez Hernandez H, Chan D, Yu AC, Stapleton LM, et al. Translational Applications of Hydrogels. Chem Rev. 22 de septiembre de 2021;121(18):11385-457.
- Jeon O, Bouhadir KH, Mansour JM, Alsberg E. Photocrosslinked alginate hydrogels with tunable biodegradation rates and mechanical properties. Biomaterials. 2009;30(14):2724-34.
- Jeon O, Alt DS, Ahmed SM, Alsberg E. The effect of oxidation on the degradation of photocrosslinkable alginate hydrogels. Biomaterials. 2012;33(13):3503-14.
- Jeon O, Samorezov JE, Alsberg E. Single and dual crosslinked oxidized methacrylated alginate/PEG hydrogels for bioadhesive applications. Acta Biomater. 2014;10(1):47-55.
- Jeong SI, Jeon O, Krebs MD, Hill MC, Alsberg E. Biodegradable photo-crosslinked alginate nanofibre scaffolds with tuneable physical properties, cell adhesivity and growth factor release. Eur Cell Mater. 2012;24:331-331.
- Ayala-Mar S, González-Valdez J. Research and Development of Emerging Technologies for Exosome-based Cancer Diagnostics and Therapeutics. 2023
- Huda MN, Nafiujjaman M, Deaguero IG, Okonkwo J, Hill ML, Kim T, et al. Potential Use of Exosomes as Diagnostic Biomarkers and in Targeted Drug Delivery: Progress in Clinical and Preclinical Applications. ACS Biomater Sci Eng. 14 de junio de 2021;7(6):2106-49.
- Wang L, Chen P, Pan Y, Wang Z, Xu J, Wu X, et al. Injectable photocurable Janus hydrogel delivering hiPSC cardiomyocyte-derived exosome for post-heart surgery adhesion reduction. Sci Adv. 4 de agosto de 2023;9(31):eadh1753.
- Liu B, Lee BW, Nakanishi K, Villasante A, Williamson R, Metz J, et al. Cardiac recovery via extended cell-free delivery of extracellular vesicles secreted by cardiomyocytes derived from induced pluripotent stem cells. Nat Biomed Eng. 2018;2(5):293-303.
- Khalatbari E, Tajabadi M, Khavandi A. Multifunctional exosome-loaded silk fibroin/alginate structure for potential wound dressing application. Mater Today Commun. 2022;31:103549-103549.
- Zhang H, Zhang J, Liu Y, Jiang Y, Li Z. Molecular Targeted Agent and Immune Checkpoint Inhibitor Co-Loaded Thermosensitive Hydrogel for Synergistic Therapy of Rectal Cancer. Front Pharmacol [Internet]. 2021;12.
- Roth JG, Brunel LG, Huang MS, Liu Y, Cai B, Sinha S, et al. Spatially controlled construction of assembloids using bioprinting. Nat Commun. 2023;14(1):4346-4346.
- Woldendorp K, Doyle MP, Bannon PG, Misfeld M, Yan TD, Santarpino G, et al. Aortic valve replacement using stented or sutureless/rapid deployment prosthesis via either full-sternotomy or a minimally invasive approach: a network meta-analysis. Ann Cardiothorac Surg. septiembre de 2020;9(5):347-63.
- Garven E, Rodell CB, Shema K, Govender K, Cassel SE, Ferrick B, et al. Tunable Blood Shunt for Neonates With Complex Congenital Heart Defects. Front Bioeng Biotechnol. 2021;9:734310-734310.
- Yetisen AK, Butt H, Volpatti LR, Pavlichenko I, Humar M, Kwok SJJ, et al. Photonic hydrogel sensors. Biotechnol Adv. 2016;34(3):250-71.
- Kim SJ, Lee G, Hong G, Yun SH, Hahn SK. Advanced light delivery materials and systems for photomedicines. Adv Drug Deliv Rev. marzo de 2023;194:114729-114729.
- Choi H, Yi J, Cho SH, Hahn SK. Multifunctional micro/nanomotors as an emerging platform for smart healthcare applications. Biomaterials. Diciembre 2021;279:121201.
- Zhao C, Park J, Root SE, Bao Z. Skin-inspired soft bioelectronic materials, devices and systems. Nat Rev Bioeng [Internet]. 17 de junio de 2024.
- Correa S, Boehnke N, Barberio AE, Deiss-Yehiely E, Shi A, Oberlton B, et al. Tuning Nanoparticle Interactions with Ovarian Cancer through Layer-by-Layer Modification of Surface Chemistry. ACS Nano. febrero de 2020;14(2):2224-37.
- Wang X, Liu S, Sun Y, Yu X, Lee SM, Cheng Q, et al. Preparation of selective organ-targeting (SORT) lipid nanoparticles (LNPs) using multiple technical methods for tissue-specific mRNA delivery. Nat Protoc. enero de 2023;18(1):265-91.
- Vander Straeten A, Sarmadi M, Daristotle JL, Kanelli M, Tostanoski LH, Collins J, et al. A microneedle vaccine printer for thermostable COVID-19 mRNA vaccines. Nat Biotechnol. 1 de marzo de 2024;42(3):510-7.
.
Autores
Sergio Antonio Ayala Mar es médico cirujano y doctor en biotecnología. Actualmente, es investigador especializado en biotecnología médica en la Escuela de Ingeniería y Ciencias del Tecnológico de Monterrey, Campus Monterrey. Es miembro del Sistema Nacional de Investigadores (SNI) nivel I. Su investigación se enfoca en el desarrollo de soluciones diagnósticas y terapéuticas utilizando tecnologías emergentes, incluyendo el desarrollo de microdispositivos y biomateriales avanzados, así como el estudio de exosomas como biomarcadores y nanotransportadores. Es autor de 9 artículos científicos (índice h:7).
José Guillermo González Valdez es Director de Vinculación y Desarrollo del Tecnológico de Monterrey. Es co-líder del Grupo de Investigación de Bioingenieria Molecular y de Sistemas de la Escuela de Ingeniería y Ciencias, Campus Monterrey. Pertenece al Sistema Nacional de Investigadores (SNI) nivel II y es autor de más de 70 artículos científicos (índice h:19).